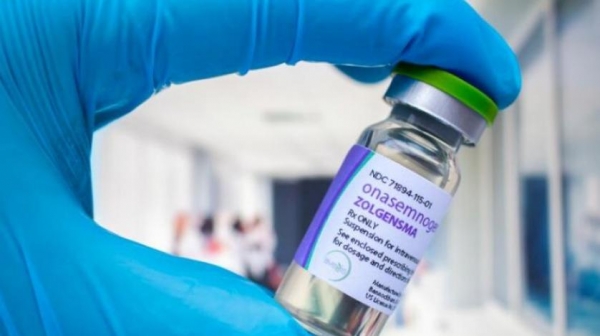
احتفل مصريون على مواقع التواصل الاجتماعي مساء أول من أمس (الجمعة)، بنجاح حملة التبرعات التي تم إطلاقها لجمع 40 مليون جنيه «نحو مليوني دولار» لتوفير أغلى دواء في العالم لطفلة تُدعى رقيّة مصابة بضمور العضلات الشوكي.
رقيّة، ليست أول طفلة مصرية تحصل على هذا الدواء المسمى «زولجينزما»، إذ سبقها طفل يدعى ريان، ولكن لم تحظَ حالة هذا الطفل بنفس قدر الاهتمام الذي أثارته حالة رقيّة، التي شارك في حملة التبرعات لها فنانون ومشاهير.
وقبل نحو عام حصل ريان على الدواء مجاناً من شركة «نوفارتيس» السويسرية، المنتجة له، وذلك في إطار حملتها لتقديم 100 فرصة للحصول على الدواء مجاناً في الدول التي لم يتم تسجيل الدواء بها، ولكن أصبح الوضع مختلفاً مع الطفلة رقيّة التي كان يتعين على أسرتها توفير هذا المبلغ الضخم لتوفير حقنة « زولجينزما» قبل بلوغها سن العامين.
ورغم تجاوب المصريين بإيجابية في التبرع للطفلة رقيّة التي كانت على بُعد أيام من بلوغها عمر العامين، حيث لا يصبح حينها العلاج مجدياً، فإن ذلك لم يمنع المصريين من التساؤل بكثافة حول سر ارتفاع ثمن هذا الدواء الذي يوصف بأنه أغلى دواء في العالم، حتى إن بعض شركات التأمين الصحي في أميركا لا تزال لا تغطيه بسبب التكلفة العالية، والبعض الآخر لديه متطلبات صارمة تحدّ من عدد المرضى المؤهلين للتغطية.
ووافقت إدارة الغذاء والدواء الأميركية في 24 مايو (أيار) من عام 2019 على هذا الدواء، ليصبح أول علاج جيني معتمد لعلاج الأطفال الذين تقل أعمارهم عن عامين المصابين بضمور عضلي في العمود الفقري (SMA)، وهو أشد أشكال ضمور العضلات الشوكي (SMA).
ويحدث ضمور العضلات الشوكي بسبب طفرة في جين الخلايا العصبية الحركية 1 (SMN1)، وهذا الجين وظيفته هي ترميز بروتين الخلايا العصبية الحركية (SMN)، وهو بروتين موجود في جميع أنحاء الجسم، وهو أمر بالغ الأهمية لصيانة وعمل الخلايا العصبية المتخصصة، والتي تسمى الخلايا العصبية الحركية.
وتتحكم الخلايا العصبية الحركية في الدماغ والحبل الشوكي في حركة العضلات بجميع أنحاء الجسم، وإذا لم يكن هناك ما يكفي من بروتين (SMN) الوظيفي، فإن الخلايا العصبية الحركية تموت، مما يؤدي إلى ضعف العضلات المميت في كثير من الأحيان، ويعاني الأطفال المصابون بهذه الحالة من مشكلات في رفع الرأس والبلع والتنفس، وقد تظهر هذه الأعراض عند الولادة أو قد تظهر في عمر 6 أشهر.
ولفهم سبب تكلفة الدواء المرتفعة، يقول تقرير نشرته مجلة «فوربس» في 16 ديسمبر (كانون الأول) من العام الماضي، إن السر يرجع إلى كيفية التصنيع، فهو من الأدوية التي تندرج تحت فئة الطب الشخصي أو الدقيق، لأنه يستهدف مشكلات معينة ناجمة عن الشفرة الجينية الفريدة للشخص، ويعد هذا النوع من الأدوية أكثر فاعلية في علاج الأمراض من الطرق التقليدية لإنتاج دواء يناسب الجميع.
وإلى جانب ذلك، فإن هذا الدواء مكلف في إعداده، فهو بشكل أكثر تحديداً يعد نوعاً من العلاج الجيني، مما يعني أنه يحل محل الجين المعيب أو غير العامل لعلاج المرض، حيث تم تصميمه لاستهداف السبب الجيني للضمور العضلي، حيث يستبدل الدواء بجين (SMN1) عند المرضى نسخةً جديدة صالحة للعمل.
ويوضح تقرير «فوربس» كيفية تسليم الجين الصحيح إلى الخلية البشرية، حيث يتم وضع الجين الجديد داخل ناقل يسمى فيروس 9 (AAV9)، وتتم إزالة الحمض النووي الفيروسي الأصلي للناقل واستبدال الجين العامل به، بحيث لا يسبب المرض، وبمجرد دخول الناقل إلى الجسم عن طريق التسريب الوريدي (IV)، يمكنه الانتقال إلى الخلايا وتوصيل الجين الجديد.
وعلى عكس علاجات الجسم المضاد التي تسمح لك بإنشاء خط خلوي لإنتاج الدواء، وتوسيع نطاق هذا الخط الخلوي إلى مفاعل حيوي سعة 10000 لتر، فإن العلاج الجيني بالطريقة التي تم وصفها مكلف للغاية في تصنيعه، والجزء المكلف من العملية، كما يكشف التقرير، هو إزالة الحمض النووي الفيروسي واستبدال الجين الصحيح المراد توصيله للجسم به.
وكما توضح إدارة الغذاء والدواء الأميركية في الصفحة الخاصة بدواء «زولجينزما» على موقعها الإلكتروني، فإن سلامة وفاعلية هذا الدواء تعتمدان على تجربة سريرية ضمّت ما مجموعه 36 مريضاً من الأطفال يعانون من ضمور العضلات الشوكي في مرحلة الطفولة والذين تتراوح أعمارهم بين أسبوعين و8 أشهر تقريباً عند دخول الدراسة.
ومقارنةً بالتاريخ الطبيعي للمرضى الذين يعانون من ضمور العضلات الشوكي في الطفولة، أظهر المرضى الذين عولجوا بـ«زولجينزما»، تحسناً كبيراً في قدرتهم الحركية، على سبيل المثال، التحكم في الرأس والقدرة على الجلوس من دون دعم.
وكانت الآثار الجانبية الأكثر شيوعاً للدواء هي ارتفاع إنزيمات الكبد والقيء، وقد يكون المرضى الذين يعانون من ضعف الكبد الموجود مسبقاً أكثر عُرضة للإصابة بإصابة خطيرة في الكبد، ويجب إكمال الفحص السريري والاختبارات المعملية لتقييم وظائف الكبد قبل العلاج بهذا الدواء، وتجب مراقبة وظائف الكبد لدى المرضى لمدة ثلاثة أشهر على الأقل بعد تناوله.
(الشرق الأوسط)